胆囊癌的预后与哪些基因和突变有关?
理研所2月22日宣布,通过对日本胆囊癌的全基因组测序分析,发现了与胆囊癌预后相关的基因和突变,并明确了其部分致癌机制。该研究由该所生物医学研究与创新中心癌症基因组研究小组组长中川英俊博士、北海道大学大学院医学研究科胃肠外科二系研究生江畑信孝博士(现为癌症基因组研究小组客座研究员)和平野聪教授带领的联合研究小组进行。该研究成果已发表在《癌症》网络版上。
胆囊癌是一种起源于胆囊上皮细胞的恶性肿瘤。 胆囊癌是由胆囊上皮细胞产生的恶性肿瘤,一般认为是由胆石症和慢性胆囊炎引起的。虽然在全世界范围内是一种罕见的癌症,但在亚洲和南美洲发生的频率很高,日本每年约有8200例。 因为它容易发生转移和侵犯,而且发生的部位复杂,周围有重要的血管,所以晚期胆囊癌的根治性手术很困难。往往无法切除,在这种情况下,5年生存率只有3%。 此外,由于对不可切除或复发的病例没有有效的治疗方法,总体5年生存率为25%,是一种极难治疗的癌症。
癌症是一种基因组疾病,它的发生和发展是由于基因组中突变的积累。 在胆囊癌中,已经发现了多种基因突变,包括肿瘤抑制基因TP53的突变。 然而,病理和遗传学有很大的差异,涉及基因组的致癌机制尚未阐明。 此外,针对癌症基因组突变的分子靶向治疗和个性化治疗的基因组突变标志物尚未完全开发。因此,有必要研究利用胆囊癌样本进行全基因组测序分析获得的基因组畸变信息与临床病理信息之间的关系。
在肿瘤微环境和免疫细胞被激活的组别中,观察到TGF-β信号相关分子的突变和异常表达
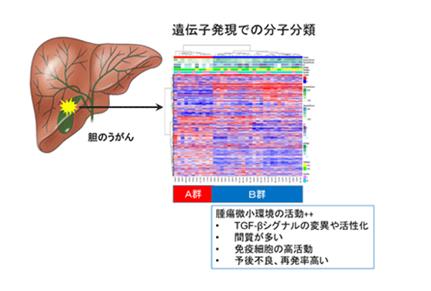
研究小组从北海道大学医院接受切除手术的36例胆囊癌的切除样本和正常组织中提取DNA,利用新一代测序仪进行全基因组测序分析或外显子组分析,寻找基因突变。 同时,从样本中提取RNA,并进行包括非编码RNA在内的RNA综合表达分析,研究胆囊癌的分子生物学特征。结果显示,胆囊癌可分为A、B两组,与A组相比,B组预后极差,且有强烈的复发倾向,在基质中观察到许多活化的成纤维细胞和具有免疫抑制功能的免疫细胞。
此外,对基因表达的途径分析显示,B组胆囊癌中与免疫、TGF-β信号转导、上皮到间质转化(ETM)相关的途径被激活。 此外,当我们比较A组和B组之间的非编码RNA的表达时,我们发现有几种microRNA在B组中高表达。 在胆囊癌细胞系中删除其中一个microRNAs,miR125B1,导致侵袭能力、EMT活性、免疫相关功能和TGF-β信号通路下降。
基因突变分析发现TP53基因、ELF3基因、SMAD4基因的突变,并检测到许多TGF-β信号相关分子的突变,尤其是B组胆管癌。 因此,这些突变可能激活TGF-β信号通路,导致EMT、肿瘤微环境的形成和免疫抑制的诱导。
有望为胆囊癌的早期诊断和联合免疫治疗的发展做出贡献
未来,本研究获得的胆囊癌基因组信息有望用于制定详细的胆囊癌分子生物学分类,推进根据分类确定治疗政策的个性化医学(癌症基因组医学)。
"此次基因组分析发现的基因突变、表达异常和免疫学改变,与胆囊癌的恶性程度和预后有关,有望促进针对尚无早期诊断或有效治疗方法的胆囊癌的新疗法的开发,尤其是联合免疫疗法。"研究组说。 该集团表示。






请您简单描述您正面临的问题和您的需求,并留下您的联系方式;
我们会为您匹配专门的医学顾问与您联系,帮你制定合适的方案。
在您提交相关的信息后,我们将会由专业的医学团队帮您规划合适的出国看病方案并进行费用预估。